AR NEWS NOTÍCIAS
Agentes causais
A triquinelose (triquinose) é causada por nematóides (lombrigas) do gênero Trichinella . Além do agente clássico T. spiralis (encontrado em todo o mundo em muitos animais carnívoros e onívoros), várias outras espécies de Trichinella são agora reconhecidas, incluindo T. pseudospiralis (mamíferos e aves em todo o mundo), T. nativa (ursos do Ártico), T. nelsoni (predadores e necrófagos africanos), T. britovi (carnívoros da Europa e Ásia ocidental) e T. papuae (porcos selvagens e domésticos, Papua Nova Guiné e Tailândia). Trichinella zimbabwensisé encontrado em crocodilos na África, mas até o momento não há associações conhecidas desta espécie com doenças humanas.
🔵 Acompanhe nosso blog site no Google News para obter as últimas notícias 📰 aqui
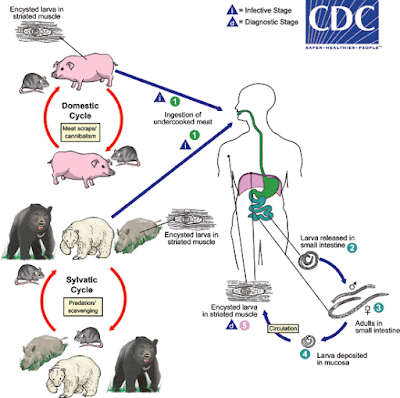 |
| Ciclo da vida da triquinela |
🟢Confira Últimas Notícias 🌎
Dependendo da classificação utilizada, existem várias espécies de Trichinella : T. spiralis , T. pseudospiralis , T. nativa , T. murelli , T. nelsoni , T. britovi , T. papuae e T. zimbabwensis , todas exceto a última dos quais têm sido implicados em doenças humanas. Vermes adultos e larvas encistadas se desenvolvem dentro de um único hospedeiro vertebrado, e um animal infectado serve como hospedeiro definitivo e potencial hospedeiro intermediário. Um segundo hospedeiro é necessário para perpetuar o ciclo de vida da Trichinella. O ciclo doméstico envolveu mais frequentemente porcos e roedores antropofílicos, mas outros animais domésticos, como cavalos, podem estar envolvidos. No ciclo silvestre, a variedade de animais infectados é grande, mas os animais mais frequentemente associados como fontes de infecção humana são ursos, alces e javalis.
A triquinelose é causada pela ingestão de carne mal cozida contendo larvas encistadas (exceto T. pseudospiralis e T. papuae , que não encistam) de espécies de TrichinellaO número 1 . Após a exposição ao ácido gástrico e à pepsina, as larvas são liberadas dos cistos O número 2e invadem a mucosa do intestino delgado, onde se desenvolvem em vermes adultos O número 3. As fêmeas têm 2,2 mm de comprimento; machos 1,2 mm. O tempo de vida no intestino delgado é de cerca de quatro semanas. Após 1 semana, as fêmeas liberam larvas O número 4que migram para os músculos estriados onde encistam O número 5. O diagnóstico geralmente é feito com base nos sintomas clínicos e é confirmado por sorologia ou identificação de larvas encistadas ou não encistadas em espécimes de biópsia ou autópsia.
Distribuição geográfica
No mundo todo. Mais comum em partes da Europa e dos Estados Unidos.
Apresentação clínica
Infecções leves podem ser assintomáticas. A invasão intestinal pode ser acompanhada por sintomas gastrointestinais (diarréia, dor abdominal, vômito). A migração larval para os tecidos musculares (uma semana após a infecção) pode causar edema periorbital e facial, conjuntivite, febre, mialgias, hemorragias em estilhaços, erupções cutâneas e eosinofilia periférica. Manifestações ocasionais com risco de vida incluem miocardite, envolvimento do sistema nervoso central e pneumonite. O encistamento larval nos músculos causa mialgia e fraqueza, seguidos de diminuição dos sintomas.
Adulto Trichinella spp. residem no trato intestinal do hospedeiro vertebrado; larvas podem ser encontradas encapsuladas no tecido muscular. O diagnóstico geralmente é feito sorologicamente ou com base na observação das larvas no tecido muscular após biópsias ou autópsias.
 |
| Figura : Larvas encistadas de Trichinella sp. em tecido muscular, corado com hematoxilina e eosina (H&E). A imagem foi capturada com ampliação de 400x. |
 |
| Figura A: Larvas de Trichinella em carne de urso prensada, parcialmente digerida com pepsina. |
Diagnóstico laboratorial
A suspeita de triquinelose (triquinose), com base na história, sintomas clínicos e eosinofilia, pode ser confirmada por testes diagnósticos específicos, incluindo detecção de anticorpos, biópsia muscular e microscopia.
Detecção de anticorpos
Os testes de imunodiagnóstico atualmente disponíveis nos EUA incluem imunoensaios enzimáticos (EIA) que detectam anticorpos específicos para Trichinella . Os EIAs utilizam preparações de antígenos que podem ser extratos brutos preparados a partir de homogenatos de larvas de músculo de T. spiralis ou produtos excretor-secretores (ES) produzidos por larvas cultivadas. O grupo TSL-1 de antígenos secretores larvais são conservados em todas as espécies/isolados de Trichinella e, portanto, podem ser usados para detectar infecção em animais ou pessoas infectadas com qualquer um dos tipos de Trichinella atualmente reconhecido. Reações positivas são detectáveis em algum momento durante a infecção em amostras de soro de 80% a 100% dos pacientes com triquinelose clinicamente sintomática (triquinose). Os níveis de anticorpos geralmente não são detectáveis até 3 a 5 semanas após a infecção, bem após o início da doença em estágio agudo. O desenvolvimento de anticorpos também é afetado pela dose infectante de larvas: quanto maior a dose infectante, mais rápida será a resposta de anticorpos do paciente. Múltiplas amostras de soro devem ser coletadas com várias semanas de intervalo para demonstrar a soroconversão em pacientes cuja amostra inicial foi negativa. Os anticorpos IgG, IgM e IgE são detectáveis em muitos pacientes; no entanto, os testes baseados em anticorpos IgG são mais sensíveis. Os níveis de anticorpos atingem o pico no segundo ou terceiro mês após a infecção e depois diminuem lentamente por vários anos.
Tratamento
O tratamento imediato com medicamentos antiparasitários pode ajudar a prevenir a progressão da triquinelose, matando os vermes adultos e evitando assim a liberação de larvas. Uma vez que as larvas se estabeleceram nas células do músculo esquelético, geralmente 3 a 4 semanas após a infecção, o tratamento pode não eliminar completamente a infecção e os sintomas associados. O tratamento com mebendazol ou albendazol é recomendado. Se o tratamento não for iniciado nos primeiros dias da infecção, podem ser necessários ciclos de tratamento mais prolongados ou repetidos. Ambas as drogas são consideradas relativamente seguras, mas têm sido associadas a efeitos colaterais, incluindo supressão da medula óssea. Pacientes em tratamentos mais longos devem ser monitorados por contagens sanguíneas completas seriadas para detectar quaisquer efeitos adversos imediatamente e descontinuar o tratamento. Albendazol e mebendazol não são aprovados para uso em mulheres grávidas ou crianças com idade inferior a 2 anos. Além da medicação antiparasitária, às vezes é necessário tratamento com esteróides em casos mais graves.
Medicamento Dose adulto e pediátrica
Albendazol 400 mg duas vezes ao dia por via oral por 8 a 14 dias
Mebendazol 200 a 400 mg três vezes ao dia por via oral por 3 dias, depois 400 a 500 mg três vezes ao dia por via oral por 10 dias
🔴Reportar uma correção ou erro de digitação e tradução :Contato ✉️













%20identificada%20em%20paciente%20dos%20EUA.jpg)


.png)









%20identificada%20em%20paciente%20dos%20EUA.jpg)






_11zon.webp)








-min.jpg)







%20identificada%20em%20paciente%20dos%20EUA.jpg)
.webp)

.png)



.webp)








.webp)




.jfif)





















